의료기기 인허가의
정밀한 설계를 약속합니다
기술문서 작성부터 품질경영시스템 구축, GMP 공장 설계까지 — 의료기기 개발의 전 주기를 아우르는 전문 컨설팅 서비스를 제공합니다.
의료기기 산업의
신뢰할 수 있는 파트너
Medqraft는 의료기기 개발 기업이 복잡한 규제 환경을 성공적으로 헤쳐나갈 수 있도록 전문적인 기술문서 및 품질문서 작성, GMP 공장 설계 서비스를 제공합니다.
식약처(KFDA) 인허가 요건부터 국제 표준(ISO 13485)까지, 의료기기 개발의 모든 단계에서 정확하고 체계적인 문서화를 통해 고객사의 제품이 시장에 빠르게 진입할 수 있도록 지원합니다.
ISO 13485, KFDA 규정에 완벽히 부합하는 기술문서 및 품질문서를 체계적으로 작성합니다.
국내외 의료기기 규제 환경에 대한 깊은 이해를 바탕으로 인허가 절차를 최적화합니다.
의료기기 제조 시설의 GMP 요건을 충족하는 공장 레이아웃과 시설 설계를 지원합니다.
개발 초기 단계부터 인허가 완료까지 전 과정을 일관되게 지원하는 통합 서비스를 제공합니다.
전문 서비스
세 가지 핵심 영역
의료기기 개발의 복잡한 규제 요건을 충족하는 맞춤형 전문 서비스를 제공합니다.

기술문서 작성
의료기기 인허가에 필요한 기술문서를 체계적으로 작성합니다. 제품 설명서, 위험관리 파일, 임상평가 보고서, 성능 시험 보고서 등 KFDA 및 국제 규격에 적합한 완전한 기술문서 패키지를 제공합니다.
- 제품 기술 사양서
- 위험관리 파일 (ISO 14971)
- 임상평가 보고서
- 성능 시험 보고서
- 사용설명서 (IFU)
품질문서 작성
ISO 13485 기반의 품질경영시스템(QMS) 구축 및 문서화를 지원합니다. 품질매뉴얼, 절차서, 지침서, 양식 등 완전한 QMS 문서 체계를 수립하여 인증 심사를 성공적으로 통과할 수 있도록 지원합니다.
- 품질매뉴얼 작성
- 표준작업절차서 (SOP)
- 설계 및 개발 절차
- 공급업체 관리 절차
- CAPA 및 불만 처리 절차
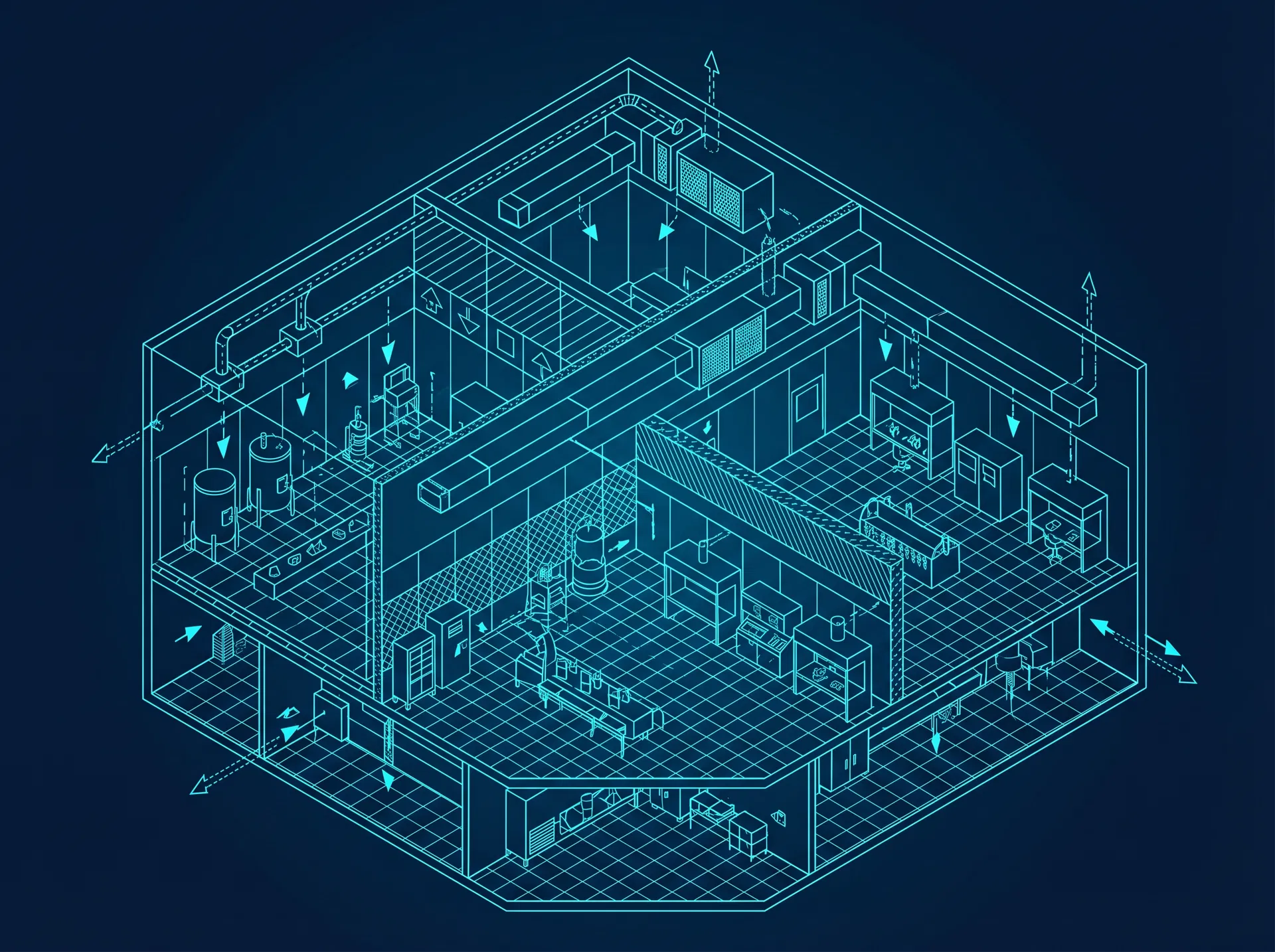
GMP 공장 설계
의료기기 제조 시설의 GMP 요건을 충족하는 공장 설계를 제공합니다. 클린룸 설계, 공기 흐름 계획, 구역 분리, 동선 설계 등 규정 준수와 생산 효율성을 동시에 달성하는 최적의 시설 레이아웃을 설계합니다.
- 클린룸 레이아웃 설계
- 공기 흐름 및 HVAC 계획
- 구역 분리 및 동선 설계
- 설비 배치 계획
- GMP 적합성 검토
체계적인 프로세스로
성공적인 인허가를 실현합니다
Medqraft는 검증된 6단계 프로세스를 통해 의료기기 인허가의 복잡성을 체계적으로 관리합니다.
초기 상담 및 분석
제품 특성과 규제 요건을 분석하고 최적의 인허가 전략을 수립합니다.
기술문서 작성
제품 설명, 위험관리, 임상평가 등 완전한 기술문서 패키지를 작성합니다.
QMS 문서 구축
ISO 13485 기반의 품질경영시스템 문서 체계를 수립합니다.
GMP 시설 설계
규정에 적합한 제조 시설 레이아웃과 환경 시스템을 설계합니다.
심사 대응 지원
인허가 심사 과정에서 발생하는 질의에 신속하고 정확하게 대응합니다.
인허가 완료
국내외 인허가를 성공적으로 완료하고 시장 진입을 지원합니다.
프로젝트를 시작할 준비가 되셨나요?
지금 바로 문의하세요
의료기기 기술문서, 품질문서 작성 또는 GMP 공장 설계에 관한 문의사항이 있으시면 언제든지 연락해 주세요. 전문 컨설턴트가 신속하게 답변드리겠습니다.
바로 메일 보내기